三阴性乳腺癌(TNBC)是一种侵袭性强、治疗选择有限的乳腺癌亚型,为众多患者和医疗团队带来严峻挑战。新的希望正在出现,一项名为Neo-N的II期临床试验,带来了突破性的发现,可能为TNBC治疗方式带来全新曙光。

此次研究由University of Newcastle的Nicholas Zdenkowski和他的团队在全球范围内12家医院(包括澳大利亚、新西兰和意大利)展开。该试验是一项由研究者发起的非对照开放标签随机II期临床试验,旨在明确探讨一种无蒽环类12周化疗方案结合不同PD-1抑制剂(纳武利尤单抗)给药时序的疗效。
研究结果令人瞩目:在12周的试验期间,无论纳武利尤单抗与化疗药物(卡铂、紫杉醇)是先导单药还是同步联用,均实现超过50%的病理完全缓解率(pCR),具体为先导组51%和同步组55%。此数据不仅为缩短疗程、降低毒性提供了新证据,还为优化免疫化疗组合策略指出了新方向,特别是对于PD-L1阳性和高TILs患者群体,这一发现尤为显著。
双时序方案的疗效对比 在论文的实验设计中,研究团队将108名早期三阴性乳腺癌患者随机分为两组,以比较两种不同免疫化疗时序方案的疗效。研究分组的目的在于检验“先导免疫”是否能够显著增强治疗效果,或者同步免疫化疗是否在整体疗效上更具优势。
其中,先导组(54人)先单用纳武利尤单抗240 mg进行免疫治疗,2周后加入卡铂及紫杉醇进行联合化疗。而同步组(54人)则是从治疗开始便同时接受纳武利尤单抗、卡铂及紫杉醇,共12周,之后再追加一次纳武利尤单抗240 mg。所有药物均通过静脉注射给药,如有需要,可使用短效粒细胞生长因子。
实验结果非常惊人:先导组51%的患者(53名中27名)和同步组55%的患者(55名中30名)均实现了病理完全缓解(pCR)。这两组实验的数据高度相似,颠覆了“先导免疫可增强疗效”的假设,表明在这一特定的免疫化疗组合中先导免疫策略并未展现出预期的显著优势(如Figure 2所示)。
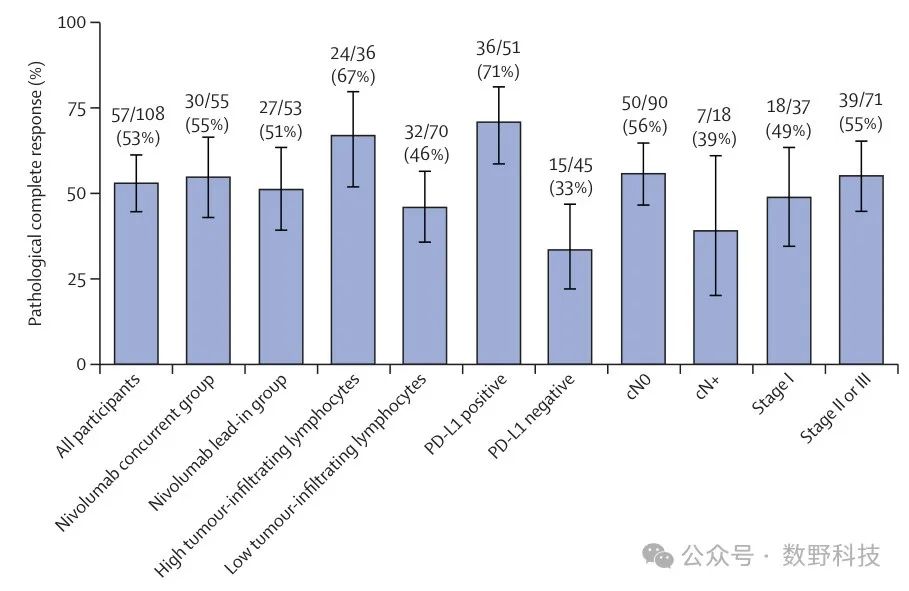
Figure 2:
研究进一步分析指出,同步组可能因化疗同步进行的协同效应,抵消了化疗的免疫抑制作用,从而与先导组在疗效上没有显著差异。该发现提示,不同药物组合和治疗时序的精确设计对于优化个体化治疗方案至关重要。未来研究还需探讨其他癌症类型中同样时序方案的有效性。如图表Table 2所示,展示了各组患者的治疗相关不良事件,而Table 3则显示了免疫相关不良事件的具体情况。
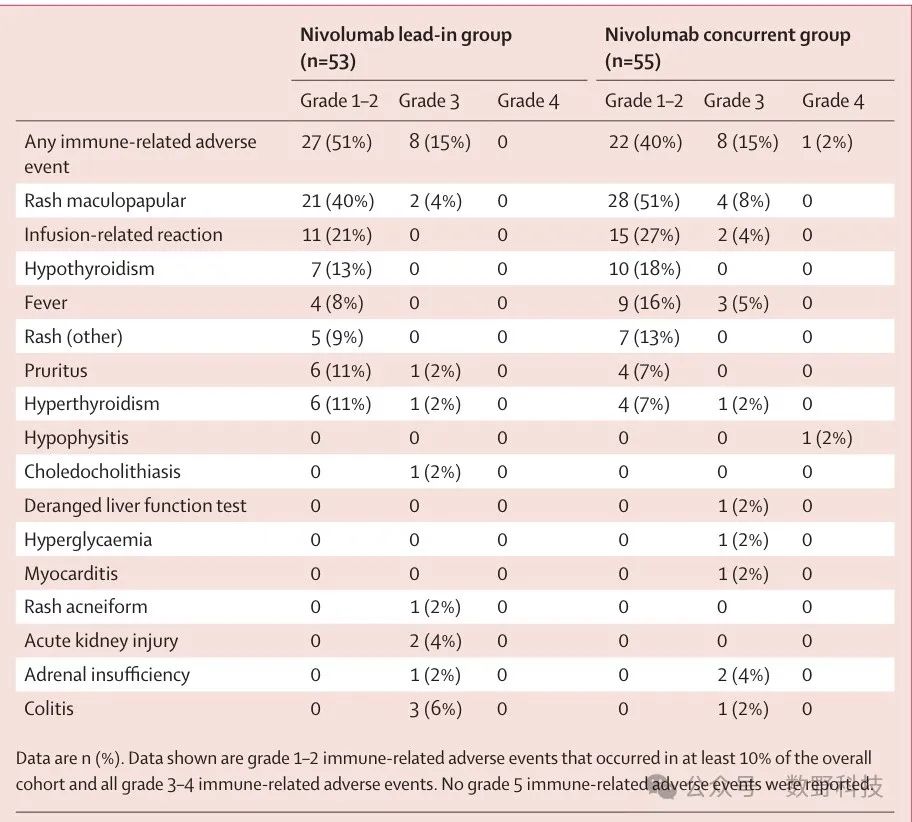
Table 3:
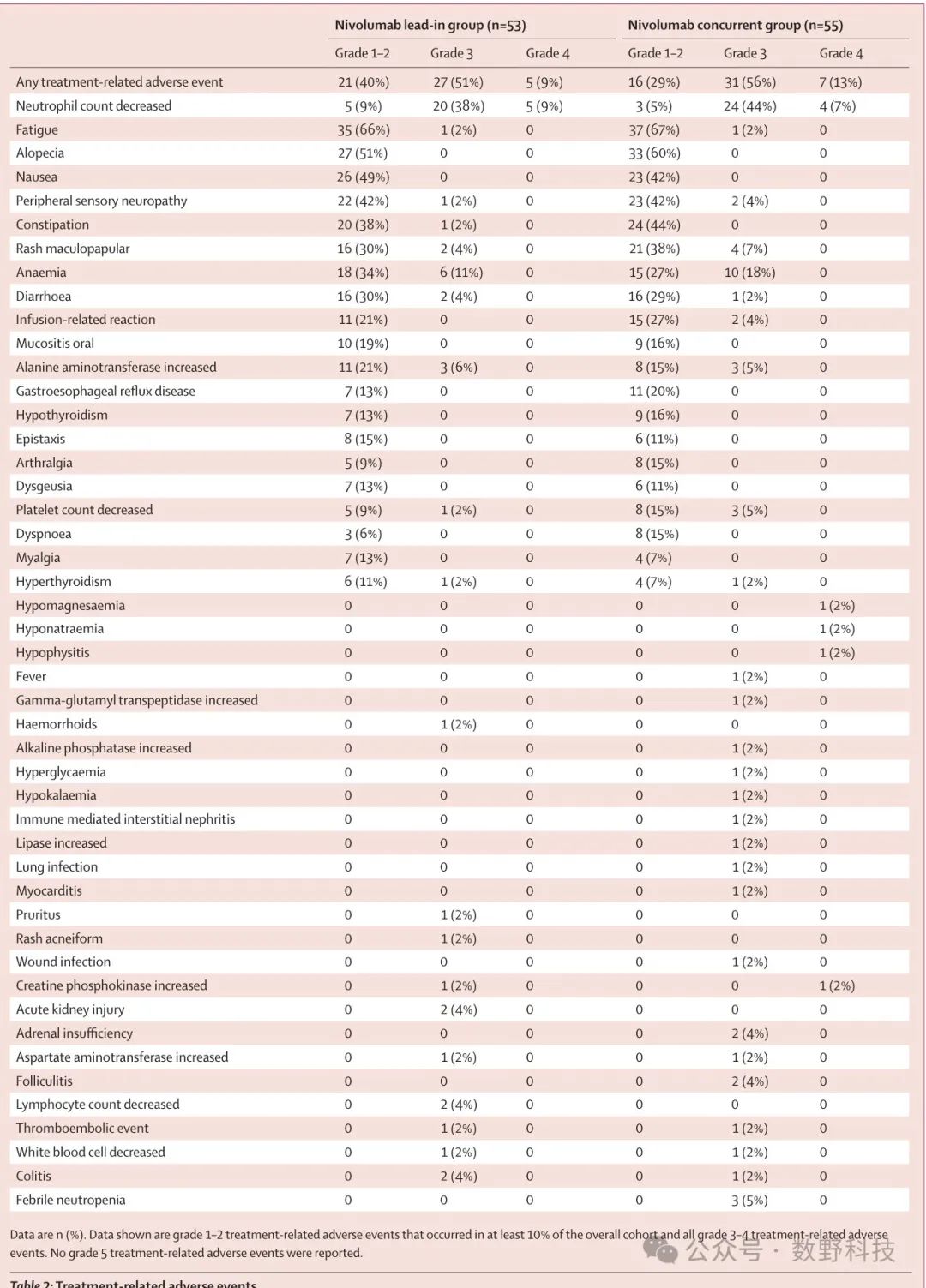
Table 2
生物标志物的关键作用 在这项研究中,生物标志物的角色尤为重要,特别是在预测患者对治疗的响应方面。研究显示,PD-L1阳性患者(定义为PD-L1表达≥1%)和拥有高肿瘤浸润淋巴细胞(TILs,定义为TILs≥30%)的患者,病理完全缓解率(pCR)显著高于其他患者组别。
研究团队对PD-L1和肿瘤浸润淋巴细胞(TILs)进行了详细分析。结果显示,PD-L1阳性患者(≥1%)中71%达到了病理完全缓解(pCR),而PD-L1阴性组仅有33%。高TILs组(≥30%)患者的病理完全缓解率达到67%,比低TILs组提升了21个百分点,这些结果在先导单药组和同步联用组中均有所体现(如图Figure 2所示)。图表Figure 2展示了不同亚组病理完全缓解率的差异情况。
值得注意的是,这些差异不仅在个别案例中显现,而是普遍存在于研究的多个子群组中。研究结果显示,高TILs和PD-L1阳性同时存在时,病理完全缓解率达到75%,而PD-L1阴性或低TILs状态的患者中,这一数字则显著降低至30%。这表明免疫微环境的特征在预测疗效中比给药时序更为重要。
通过生物标志物指导下的治疗方案优化,使我们能够更加精准地筛选出对治疗最具响应潜力的患者群体。这不仅提高了治疗效率,还为未来个体化治疗策略提供了坚实的科学依据。在这项研究的基础上,下一步的实验会更关注于系统性验证这些生物标志物在不同治疗方案中的作用,并探索新的生物标志物,以进一步提升患者的治疗效果。
安全性及实施可行性 这项研究还详细探讨了12周短疗程无蒽环化疗方案的安全性及实施可行性。引入新的疗法不仅需要考虑疗效,还需仔细评估其安全性和患者的依从性,以确保临床实践中的可行性和广泛应用。
在这项研究中,65%的患者经历了3-4级的不良事件,主要包括中性粒细胞减少(占47-53%)和贫血(占11-19%)。这些数据强调了监测和管理这些副作用的必要性,以便患者能够完成整个治疗过程。中性粒细胞减少和贫血的不良事件详细数据如图表Table 2所示,展示了治疗相关不良事件的具体统计。
尽管同步组患者的严重不良事件发生率较高(47% vs 30%),但94%的患者能够完成计划的免疫剂量,这表明12周短疗程具有良好依从性,并为替代传统的24周方案奠定了基础。如图Table 2所示,展示了不同治疗组中患者的完成情况和具体不良事件情况。
综合来看,12周无蒽环短疗程不仅在疗效上具有优势,在安全性和患者依从性方面也表现出良好的潜力。这为在临床中推广和实施更短疗程的免疫化疗方案提供了重要依据。接下来的研究有望进一步验证这些发现,并优化治疗方案,以便能够更广泛地应用于三阴性乳腺癌患者。
结语 Neo-N试验的突破性数据不仅改写了三阴性乳腺癌的治疗逻辑,更揭示了免疫微环境的核心地位——PD-L1阳性与高TILs患者病理完全缓解率分别达到71%和67%,这意味着未来可能仅需12周无蒽环短疗程即可为特定人群实现高效治疗。当传统24周含蒽环方案仍在引发中性粒细胞减少(53%)、贫血(19%)等毒性时,这项研究已证明:精准筛选优势人群的治疗降阶梯策略,既能保留疗效(总体pCR 53%),又能大幅减少患者暴露于长期毒性的风险。
这项成果引发的思考比答案更多:当III期试验验证等效性后,是否所有患者都应转向短疗程?PD-L1/TILs阴性患者33%的pCR是否暗示需要更激进方案?同步组虽实现55%缓解率,但47%的严重不良事件率提醒我们——免疫化疗的时序优化仍需精细平衡疗效与毒性。而最令人期待的长期随访数据,将回答一个根本问题:12周短疗程带来的病理缓解,能否转化为与24周标准方案等同的生存获益?
此刻我们正站在治疗范式转换的临界点:94%患者完成免疫剂量的数据证实了短疗程的临床可行性,而生物标志物指导的阶梯式治疗策略(如对PD-L1阴性患者的升级治疗)可能成为新的标准。这不仅是三阴性乳腺癌治疗的转折点,更为实体瘤治疗指明了方向——当精准医学遇见治疗降阶梯,我们正在见证’少即是多’治疗哲学的最佳实践。
参考文献:
[1] Timing of nivolumab with neoadjuvant carboplatin and paclitaxel for early triple-negative breast cancer (BCT1902/IBCSG 61–20; Neo-N): a non-comparative, open-label, randomised, phase 2 trial Zdenkowski, Nicholas et al. The Lancet Oncology, Volume 26, Issue 3, 367 – 377 https://doi.org/10.1016/S1470-2045(24)00757-5
