重症肌无力是一种非常罕见的慢性自身免疫性疾病,它会逐渐削弱患者的肌肉力量,严重影响日常生活。尽管现有治疗方法多样,但许多患者仍面临疗效有限或副作用严重的困境。

近期,《Lancet Neurology》发表了一项由全球多个中心联合进行的3期临床试验 LUMINESCE,首次评估了 IL-6 受体抑制剂 satralizumab 在治疗全身性重症肌无力中的安全性和有效性。该研究由来自加州大学尔湾分校、复旦大学附属华山医院及其他多家国际知名机构的研究团队共同实施,涵盖了105个研究中心。
研究发现,satralizumab 在24周时展现出统计学显著的临床改善,有效降低了MG-ADL评分。satralizumab组的调整均值为-3.59分,相比之下安慰剂组的调整均值为-2.57分,两者改善差值为1.02分。此外,安全性特征与安慰剂相当,不良事件的发生率稍高但无显著差异(satralizumab组90%,安慰剂组73%)。这项研究不仅为 IL-6 信号通路在自身抗体介导疾病中的作用提供了新的证据,同时也为重症肌无力治疗开辟了新的方向。
全球多中心试验设计
为了探索satralizumab在重症肌无力治疗中的疗效和安全性,该研究采用了严格的全球多中心试验设计。试验共纳入了188例乙酰胆碱受体抗体阳性患者,包括105个来自欧洲、北美洲、南美洲、澳大利亚和亚洲的研究中心(如图Figure 1所示)。
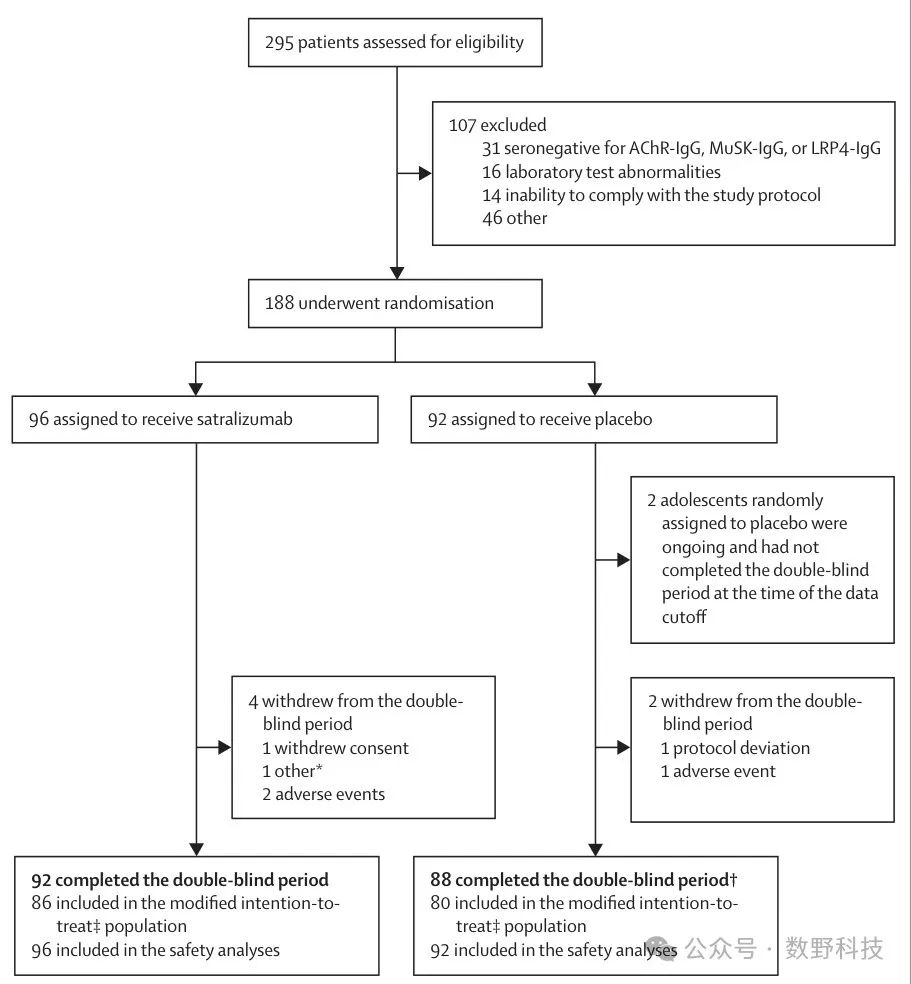
Figure 1
研究参与者被随机分配至satralizumab组或安慰剂组。按照基线体重进行分层给药:体重≤100kg的患者每次皮下注射120mg,体重>100kg的患者每次皮下注射180mg。按照四周一次的频率进行长达24周的治疗。
该试验设计独特之处在于采用了双盲设计和双评估模式。研究团队通过独立的网络系统随机分配患者,并确保研究者、患者及赞助方对患者分配的治疗组都不知情。同时采用预灌装注射器进行satralizumab和安慰剂的注射,使得两者外观和包装完全一致,进一步巩固了盲法的实施。
为确保疗效评估与治疗决策的独立性,试验中引入了治疗医生和评估医生的角色区分。治疗医生负责患者的安全评估和治疗决策,而评估医生则专注于疗效的评估。这种双评估模式最大限度减少了偏倚,提升了研究结果的可靠性。
临床终点的改善分析
让我们深入探讨下具体的临床终点评估。临床试验的主要终点是评估基础至24周时的MG-ADL评分变化,这是一项用于评估患者日常生活活动能力的评分。
在24周时,satralizumab组的患者在这一评分上有显著改善,较基线下降了3.59分,而安慰剂组仅下降了2.57分,这一差异具有统计学显著性(p=0.020)(如图Figure 2所示)。图中展示了从基线到第24周MG-ADL总评分的变化情况,其中蓝色曲线代表satralizumab组,红色曲线代表安慰剂组,可以清楚地看到satralizumab组的评分下降幅度更大。
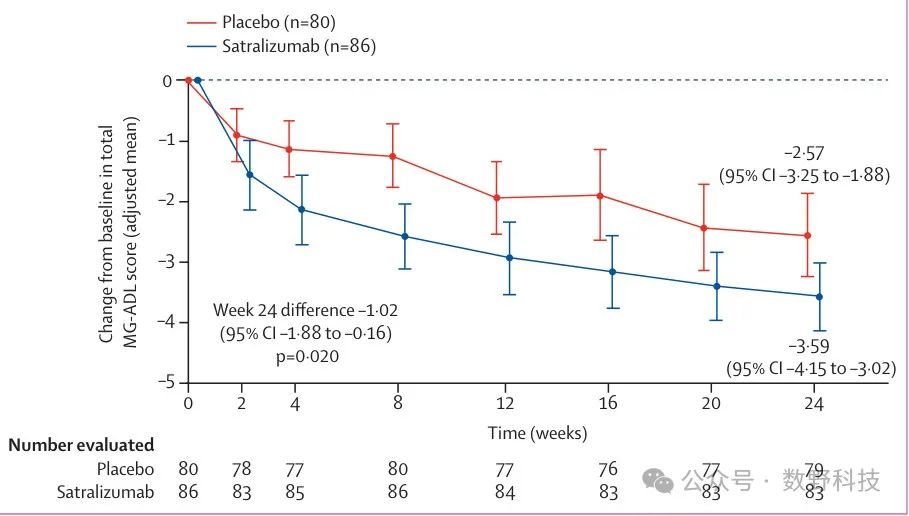
Figure 2
次要终点QMG评分也表现出相似趋势,satralizumab组较基线改善了3.35分,而安慰剂组改善为2.24分。然而,患者生活质量评分(MG-QoL15r)并未表现出显著差异(p=0.11),这表明尽管有些患者在功能上显著改善,总体的生活质量变化不明显。
更为重要的是,虽然仅有48%的患者达到QMG评分改善3分以上的临床显著改善标准,但这提示了Satralizumab在治疗重症肌无力方面的潜力。研究人员指出,这一结果为未来筛选获益人群以及进一步优化治疗方案提供了重要线索。
安全性特征解析
根据研究,satralizumab 组的患者中有 90%(86名患者)发生了不良事件,略高于安慰剂组的 73%(67名患者)(如图Table 3所示)。表内详细列出了不良事件的类型及其发生频率。
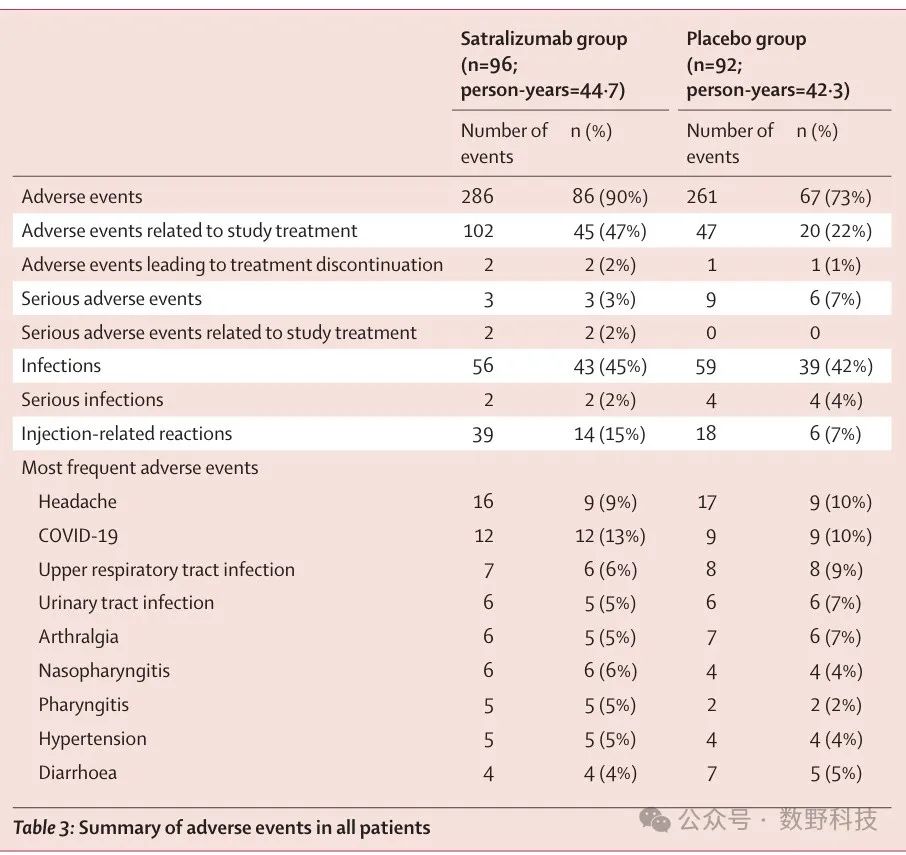
Table 3
研究表明,satralizumab 组共有 86 例患者(90%)发生了至少一次不良事件,略高于安慰剂组的 67 例患者(73%)。然而,两组之间的严重不良事件发生率相似,分别为3%(satralizumab组)和7%(安慰剂组)。数据显示在表 Table 3 中,有助于理解不同类型和频率的不良事件。
最常见的不良反应包括头痛、上呼吸道感染和注射部位反应。这些不良事件的总体发生率较低且大多为轻度或中度。如图表 Table 3 所示,进一步细分了各类不良反应的发生率。
值得注意的是,satralizumab 组和安慰剂组均未出现药物相关性肝损伤或死亡事件。这与先前的神经脊髓炎研究结果一致,进一步验证了 satralizumab 的安全性。
结语
这项研究揭示了一个关键转折点:IL-6通路抑制为重症肌无力治疗打开了新的维度。尽管3.59分与2.57分的MG-ADL评分差异看似微小,但48%的患者达到QMG显著改善的亚组数据提示,精准筛选获益人群可能让疗效产生质的飞跃。当其他生物制剂聚焦补体系统时,satralizumab通过调节上游免疫信号另辟蹊径,这种机制创新或将重塑自身免疫疾病的治疗格局。
值得深思的是,研究揭示的「有限改善」与「显著安全优势」形成微妙平衡——90%不良事件发生率中仅3%为严重事件,且无药物相关死亡。这提示我们:在慢性病管理中,温和但持久的免疫调节可能比激进治疗更具临床价值。未来若能将IL-6抑制与现有疗法形成「免疫调节组合拳」,或许能在安全边际内突破疗效天花板。
从更宏大的视角看,IL-6通路在神经免疫领域的「跨界」验证尤为振奋。当同一靶点在神经脊髓炎和重症肌无力中相继奏效,是否意味着存在跨疾病的共同免疫开关?这项研究不仅是药物开发的故事,更是对「精准免疫调节」理论的强有力佐证——或许我们距离解码神经-免疫对话的通用密码,又近了一步。
参考文献
[1] Habib, A. A., Zhao, C., Aban, I., França, M. C., Jr, José, J. G., Zu Hörste, G. M., Klimiec-Moskal, E., Pulley, M. T., Tavolini, D., Krumova, P., Lennon-Chrimes, S., Smith, J., Thanei, G. A., Blondeau, K., Vodopivec, I., Wolfe, G. I., & Murai, H. (2025). Safety and efficacy of satralizumab in patients with generalised myasthenia gravis (LUMINESCE): a randomised, double-blind, multicentre, placebo-controlled phase 3 trial. The Lancet. Neurology, 24(2), 117–127. https://doi.org/10.1016/S1474-4422(24)00514-3IF: 46.5 Q1
